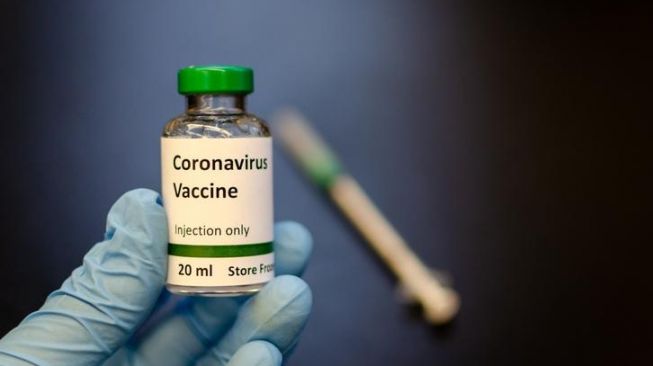
Suara.com - Menanggapi Brasil yang menangguhkan vaksin Covid-19 buatan perusahaan farmasi China, Sinovac, karena adanya Kejadian Ikutan Pasca Imunisasi (KIPI) serius atau Serious Adverse Event (SAE), Bio Farma memastikan akan meminta investigasi lebih lanjut.
SAE adalah salah satu dari KIPI yang serius dan dialami oleh penerima obat atau vaksin, tanpa memandang hubungannya dengan obat atau vaksin tersebut.
Sedangkan KIPI non serius atau KIPI ringan adalah kejadian medis yang terjadi setelah imunisasi, tapi tidak menimbulkan risiko potensial pada kesehatan si penerima seperti terjadi demam, bengkak di lokasi suntikan, atau memerah di lokasi suntikan.
Ahli Farmakovigilan Bio Farma, Novilia mengatakan investigasi harus dilakukan untuk memastikan sebab SAE yang terjadi. Apakah disebabkan oleh vaksin atau bukan vaksin sinovac (co-incident).
"Dalam penyelidikan SAE ini, otoritas Badan Pengawas Obat setempat tentu akan dilibatkan," jelas Novilia berdasarkan keterangan tertulis yang diterima suara.com, Rabu (11/11/2020).
Menurut Novilia jeda atau penangguhan dalam uji klinis vaksin, seperti yang dilakukan Brasil adalah prosedur normal dan biasa, umumnya dilakukan untuk mencari tahu penyebab KIPI serius yang dialami relawan dalam pengujian atau penelitian.
Lebih jauh Sinovac sendiri disebut sudah melakukan komunikasi dengan Butantan Institute dan menyatakan jika kejadian SAE di Brasil tidak ditemukan berhubungan dengan vaksin (co-incident).
Butantan Institute adalah salah satu perusahaan farmasi terkemuka di Brasil yang rencananya akan bekerjasama memproduksi 46 juta dosis vaksin Covid-19, yang dikembangkan perusahaan farmasi China, Sinovac.
Butantan Institute tetap bersikukuh menjalankan rencananya meski Presiden Brasil, Jair Bolsonaro mengatakan tidak akan membeli vaksin dari Sinovac. Padahal menteri kesehatan negara itu sudah memasukkan vaksin Sinovac menjadi produk vaksin yang akan digunakan untuk imunisasi Covid-19 di Brasil.