Suara.com - Kepala Badan Pengawas Obat dan Makanan (BPOM) Taruna Ikrar mengungkap 5 tempat uji klinik vaksin tuberkulosis (TBC) kerja sama Bill Gates di Indonesia. Di mana saja, dan apa saja ya manfaat Indonesia jadi tempat uji klinik fase 3 vaksin M72/AS01E-4 alias vaksin M72?
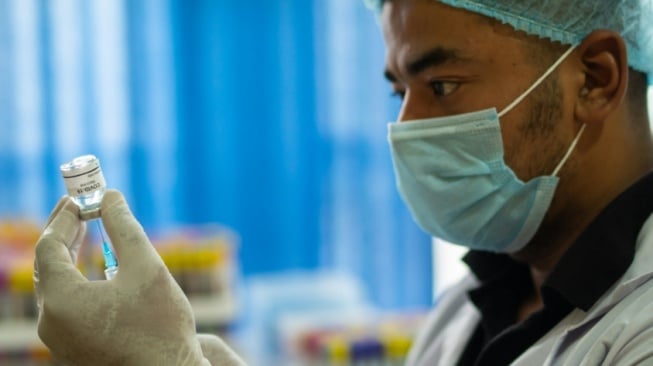
Dalam konferensi pers pada Kamis, (15/5/2025) lalu Taruna mengatakan vaksin M72 adalah vaksin tuberculosis recombinant fusion protein yang dikembangkan oleh GlaxoSmithKline Biologicals, SA (GSK).
Adapun sentra uji klinik fase 3 vaksin tuberkulosis yaitu Rumah Sakit Umum Pusat (RSUP) Persahabatan, RS Universitas Indonesia, Research Center for Care and Control of Infectious Disease (RC3ID) Universitas Padjadjaran, RS Islam Jakarta Cempaka Putih, dan Fakultas Kedokteran Universitas Indonesia.
Sebanyak 2.095 orang di Indonesia bakal jadi subjek uji klinik oleh PT Bio Farma sebagai peneliti. Rencananya ada 20.000 orang di seluruh dunia yang bakal jadi target uji klinik. Selain di Indonesia, penelitian ini juga dilakukan di Vietnam, Afrika Selatan, Malawi, Kenya, Mozambik, dan Zambia.
Sebagai negara dengan jumlah kasus tuberkulosis atau TBC terbanyak kedua di dunia, kata Taruna Indonesia bakal dapat keuntungan dengan lebih mudahnya mengendalikan TBC di Tanah Air yang sudah menjadi penyakit laten.
"Apa untungnya bagi Indonesia? Berdasarkan epidemiologi, penyakit TB terbesar kedua di dunia adalah Indonesia, setelah India. Artinya, rakyat Indonesia sangat butuh pengobatan TBC. Kita butuh variasi pengobatan baru, dengan penemuan ini, dampaknya akan bermanfaat bagi masyarakat Indonesia,” lanjutnya.
Di sisi lain, sebelum memasuki uji klinis vaksin TBC fase 3, vaksin ini juga sudah lebih dulu melalui proses peer-review oleh tim independen dari Komite Nasional Penilai Obat (KOMNAS Penilai Obat) yang telah mengamati secara saksama terhadap hasil uji pra-klinik serta uji klinik fase 1 dan 2.
"Dari hasil evaluasi tersebut, maka tim independen berdasarkan keilmuannya melaporkan hasil rekomendasi kepada BPOM, bahwa [vaksin M72] telah memenuhi semua unsur-unsur persyaratan, baik etik, saintifik, dan keamanan dari vaksin tersebut,” tambah Taruna.
Perlu diketahui, menurut situs CDC disebutkan uji klinis fase 3 untuk vaksin adalah tahap pengujian vaksin cakupannya diperluas antara 1.000 hingga 3.000 orang. Pada tahap ini peneliti nantinya akan mengonfirmasi seberapa baik vaksin bekerja, memantau efek samping yang umum dan kurang umum, serta mengumpulkan informasi untuk mendukung penggunaan yang aman pada manusia.
Sebelum fase 3, demi keamanan vaksin juga akan lebih dulu menjalani uji klinis tahap 1 yaitu diberikan pada kelompok kecil, antara 20 hingga 100 orang untuk melihat seberapa aman vaksin diberikan pada manusia, serta melihat efek samping dan memantau respons kekebalan tubuh.
Selanjutnya uji klinis tahap 2 yaitu pada 100 hingga 300 orang dengan usia dan kesehatan fisik tertentu untuk mewakili populasi. Di fase ini akan dilihat keselamatan tambahan dan risikonya.
Setelah uji klinis fase 3 selesai, barulah tahap 4 yaitu persetujuan FDA, vaksin ini dinyatakan bisa digunakan pada masyarakat umum.
Tuberkulosis adalah penyakit menular yang disebabkan oleh bakteri Mycobacterium tuberculosis. Biasanya menyerang paru-paru, namun dapat juga menyerang organ tubuh lainnya.
Sebagai catatan, Indonesia jadi negara pemilik kasus TBC terbanyak kedua setelah India, yaitu 1.060.000 kasus TBC dengan memakan korban jiwa 134.000 setiap tahunnya. Ini artinya, di Tanah Air terdapat 17 orang meninggal karena tuberkulosis setiap jam-nya.
Meski sudah jadi penyakit laten, pengendalian tuberkulosis di Indonesia masih saja belum berhasil, padahal pemerintah sudah menerbitkan Peraturan Presiden No. 67 Tahun 2021 tentang Penanggulangan TBC tapi hasilnya belum memuaskan.
Bahkan tidak sedikit orang yang menganggap remeh penyakit ini. Padahal jika sudah terdeteksi, penderitanya perlu mengonsumsi obat TBC setiap hari tanpa berhenti minimal selama 6 bulan hingga tahunan.
Ditambah pasien TBC juga kerap dihadapkan pada stigma dari masyarakat sekitar. Apalagi bakteri tuberkulosis bukan hanya menyerang saluran pernapasan tapi juga bisa menginfeksi organ vital lain, seperti otak, tulang, kulit, ginjal, hingga jantung.