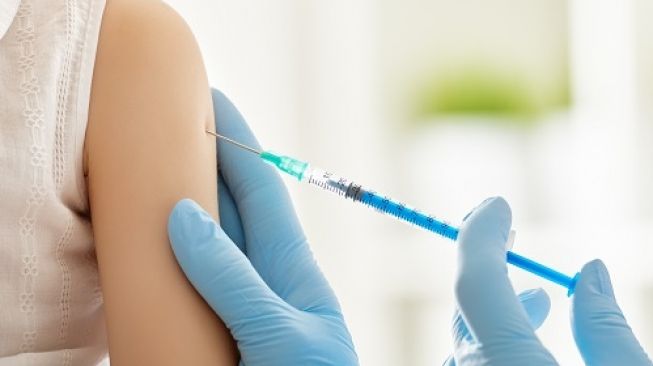
Suara.com - Amerika Serikat tengah mempertimbangkan izin penggunaan vaksin Covid-19 pertama bagi anak balita atau anak-anak di bawah usia 5 tahun. Langkah itu dilakukan setelah Pfizer Inc dan BioNTech SE mulai mengajukan permohonan izin pada Selasa (1/2/2022).
Anak balita merupakan satu-satunya kelompok usia yang belum tercakup dalam program vaksinasi Covid-19. Kehadiran vaksin bagi balita ini diharapkan dapat membantu para orangtua yang harus menghadapi karantina dan penutupan tempat-tempat pra-sekolah dan penitipan anak.
"Memiliki vaksin yang aman dan efektif bagi anak-anak di kelompok usia ini menjadi prioritas," kata penjabat Komisaris FDA Janet Woodcock, mengutip Reuters.
Pfizer Inc dan BioNTech SE mulai mengajukan data untuk izin penggunaan darurat meskipun mereka belum memenuhi target penting dalam uji klinis terhadap kelompok usia 2-4 tahun.
Pengajuan data dilakukan atas permintaan Badan Pengawas Obat dan Makanan AS (FDA) untuk memenuhi kebutuhan mendesak di sektor kesehatan publik bagi kelompok usia tersebut, kata mereka.
Pfizer dan BioNTech mengatakan mereka meminta persetujuan FDA atas penggunaan dua dosis pertama dari rejimen tiga-dosis vaksin buatan mereka. Dan keputusan tentang hal itu diharapkan akan keluar paling cepat bulan ini.
"Jika dua dosis diizinkan, para orangtua akan punya kesempatan untuk mulai mengimunisasi anak-anak mereka dengan vaksin Covid-19 sambil menunggu persetujuan bagi dosis ketiga," kata CEO Pfizer Albert Bourla, mengutip dari Antara.
Dia mengatakan, perusahaannya yakin tiga dosis vaksin akan diperlukan "untuk mencapai level perlindungan tinggi terhadap varian saat ini dan di masa depan".
Kedua perusahaan diharapkan dapat menyelesaikan pengajuan data ke FDA dalam beberapa hari mendatang. Data tentang dosis ketiga akan diajukan kemudian.
Pfizer dan BioNTech tengah menguji dosis 3 mikrogram vaksin pada kelompok usia balita. Dosis itu lebih rendah dari 10 mikrogram vaksin untuk anak 5-11 tahun dan 30 mikrogram untuk anak usia 12 tahun ke atas.
Kedua perusahaan mengatakan mereka berharap memiliki pasokan dosis 3 mikrogram yang cukup jika FDA mengizinkan vaksin tersebut.
Pengajuan izin oleh Pfizer-BioNTech dapat mempercepat vaksinasi bagi kelompok usia balita bulan ini.
Pfizer saat ini sedang menguji dua dosis dengan jarak waktu tiga pekan, diikuti dengan dosis ketiga minimal delapan pekan kemudian.
Pada Desember, Pfizer mengatakan pihaknya sedang mengubah percobaan klinisnya untuk menguji versi tiga-dosis dari vaksin tersebut karena dosis rendah menghasilkan respons kekebalan yang lebih lemah pada anak usia 2-4 tahun dibandingkan respons pada usia 16-25 tahun.
Pada anak usia 6 bulan hingga 24 bulan, vaksin tersebut memicu respons kekebalan yang setara dengan usia 16-25 tahun.