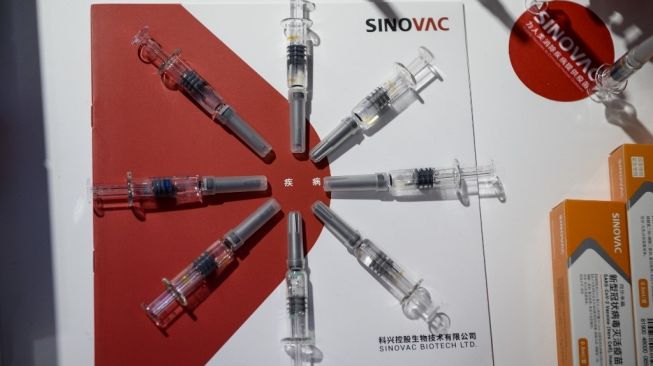
Suara.com - Indonesia turut andil dalam penelitian pembuatan vaksin Sinovac untuk Covid-19 buatan China.
Penelitian di Indonesia mulai dilakukan saat sudah memasuki fase 3, sedangkan uji klinis fase 1 dan 2 hanya dilakukan di China.
Selain Indonesia, Brasil dan Turki juga melakukan penelitian serupa pada uji klinis fase 3. Hasil penelitian akan digabungkan untuk nantinya dijadikan vaksin Covid-19.
Nantinya, Indonesia akan menggunakan vaksin Sinovac tersebut. Namun sebelum diedarkan ke masyarakat Indonesia, vaksin tersebut harus mendapatkan izin edar dan penggunaan dari Badan Pengawasan Obat dan Makanan (BPOM).
Pelaksana tugas Deputi Pengawasan Obat, NAPZA BPOM Dra. Togi. J. Hustadjulu menyampaikan bahwa BPOM tetap bisa menerbitkan izin walaupun penelitian vaksin dilakukan diberbagai negara.
"Uji klinik memang Sinovac dilakukan multicenter ada di Brasil, Turki, Indonesia untuk fase 3. Fase 1 dan fase 2 dilakukan di Tiongkok. Uji klinik pada dasarnya bisa kita terima hasilnya dari berbagai negara," kata Togi dalam konferensi pers virtual, Rabu (38/10/2020).
"Karena ini merupakan suatu standar umum dalam rangka pemberian persetujuan emergency use maupun dalam pemberian izin edar, jadi hasil uji klinis dari negara lain bisa digunakan BPOM," tambahnya.
Menurutnya, negara lain juga walaupun tidak turut andil dalam pebelitian uji klinis, tetapi bisa memberikan izin edar dan penggunaan obat dalam rangka penyembuhan maupun pencegahan suatu penyakit.
Togi menjelaskan, emergency use merupakan mekanisme registrasi khusus untuk obat dan vaksin pada kondisi darurat seperti pandemi Covid-19. BPOM bisa menggunakan persetujuan penggunaan darurat jika sudah berdasarkan evaluasi uji klinis dan hasil pembuatan obat untuk memenuhi aspek.
"Pemberian penggunaan obat dalam kondisi darurat ini harus dengan pertimbangan kemanfaatan yang lebih tinggi dari risikonya. Dalam memberikan persetujuan penggunaan obat dan vaksin BPOM dapat peroleh data dari uji klinis yang dilakukan di Indonesia maupun data yang diperoleh dari uji negara lain dengan pelaksaan uji klinis yang sama," paparnya.
"Data bisa menjadi tambahan pendukung terkait untuk khasiat dan keamann sambil menunggu hasil uji klinis fase 3 selesai dengan lengkap," tambah Togi.
Togi mengungkapkan, uji klinis fase 3 vaksin Sinovac di Indonesia telah memasuki tahap intern untuk ditargetkan selesai akhir tahun ini. Kemudian laporan hasil penelitian akan diberikan ke BPOM pada Januari 2021.